En un estudio reciente publicado en bioRxiv* Servidor de preimpresión, los investigadores examinaron diferentes anticuerpos monoclonales (mAb) para seleccionar el mAb óptimo con mayor afinidad de unión al dominio de unión al receptor (RBD) de las proteínas del síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2) de diferentes variantes usando en silico Que se acerca.
estancia: Hacia un anticuerpo monoclonal ideal con mayor afinidad de unión al dominio de unión al receptor de las proteínas SARS-CoV-2 circulantes de diferentes variantes. Haber de imagen: Kateryna Kon/Shutterstock.com
antecedentes
La pandemia en curso causada por el SARS-CoV-2 ha infectado a más de 311 millones de personas en todo el mundo y ha causado más de 5,5 millones de muertes hasta el momento. Aunque el rápido desarrollo y la rápida distribución de las vacunas contra la enfermedad por coronavirus 2019 (COVID-19) han reducido efectivamente los resultados graves del SARS-CoV-2, un gran número de personas aún no están vacunadas debido al acceso desigual a la vacuna en muchas partes del mundo.
Por lo tanto, es necesaria una nueva investigación sobre genómica, estructura y dinámica molecular, mecanismos de asociación y ciclo de vida de la infección por SARS-CoV-2 para encontrar estrategias efectivas para tratar COVID-19.
sobre estudiar
En este estudio, los investigadores evaluaron diferentes interacciones complejas antígeno-anticuerpo (Ag-Ab) utilizando un software de diseño de anticuerpos seguido de cálculos de Monte Carlo (MC) de pH constante y cálculos de dinámica molecular de carga fija gruesa (CG). , y una simulación MD atómica con carga fija. Estos estudios se realizaron en un intento de identificar un candidato Ab con una afinidad relativamente mayor en los cuatro tipos de evaluación utilizando el complejo RBD-CR3022 experimental actual como plantilla.
El ensayo inicial se realizó utilizando el software de estructura de anticuerpos diseñado por ROSETTA. Según su función de puntuación, los investigadores clasificaron 235.000 candidatos, de los cuales solo 383 mostraron afinidades mejoradas en comparación con el complejo CR3022-RBD.
Entre los 383 candidatos, los investigadores seleccionaron diez complejos Ag-Ab que mostraron la mejor afinidad en todos los cálculos teóricos. Los diez candidatos seleccionados fueron evaluados adicionalmente mediante cálculos de energía libre (G) usando muestreo universal (US) y FORTE.
Resultados
Los cálculos de la energía libre del complejo RBD-Ab para diez candidatos seleccionados mediante el método de muestreo del dosel mostraron que P01, P05, P06, P09 y P10 mejoraron significativamente la afinidad de unión en comparación con CR3022. El valor de energía libre fue de -18,3 kcal/mol para P01 y de -7,1 kcal/mol a -10,8 kcal/mol para el grupo P01-P05-P06-P09-P10 en relación con el anticuerpo CR3022 de tipo salvaje. P01 mostró la mejor y mejor afinidad de unión en comparación con el CR3022 original y la combinación de P05, P06, P09 y P10.
Se observó que los cálculos de la energía de enlace libre de RBD-Ab por FORTE para diez candidatos seleccionados fueron del orden de P01/P06>P02/P05/P08/P09/P10>P04>P03>P05. Esto indicó a P01 y P06 como los mejores candidatos con valores de energía libre de -0,788 kb y -0,790 kb, respectivamente.
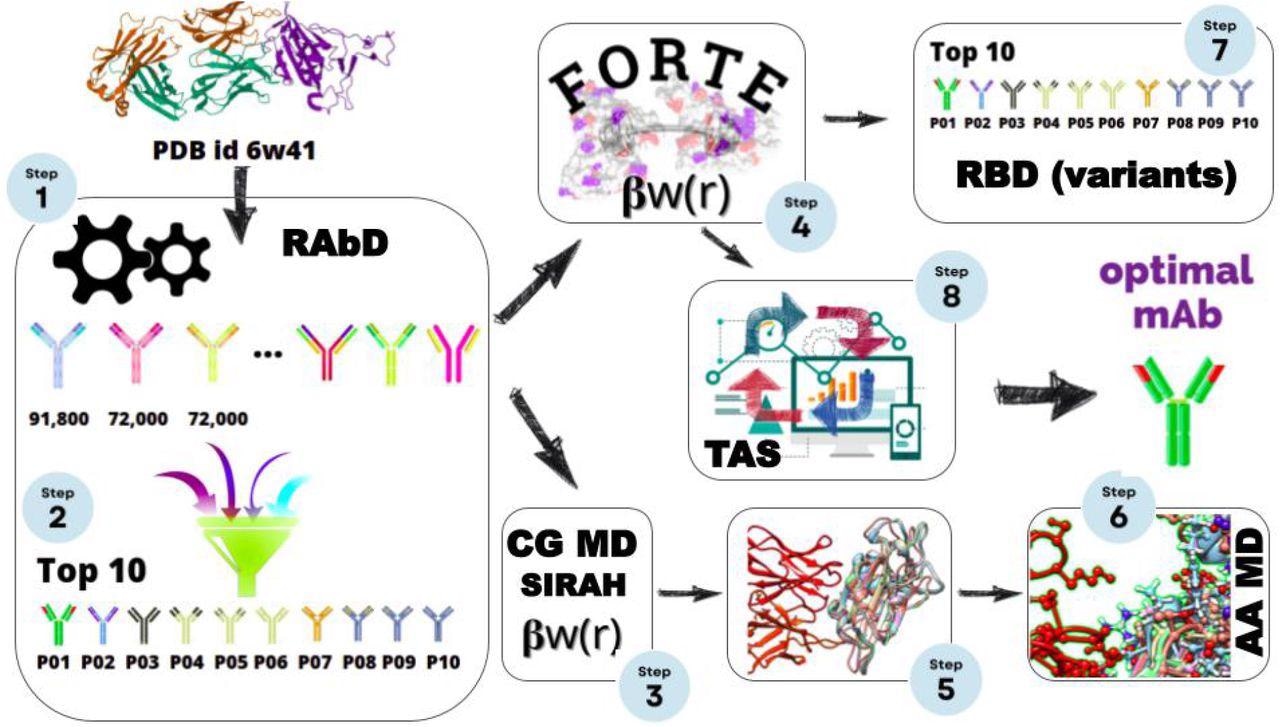
Esquema de protocolo multiescala in silico, que consiste en una metodología elemental basada en bioinformática estructural para explorar macromoléculas como posibles candidatos (Pasos 1 y 2), CG MD con carga estática (Pasos 3 y 5), simulación de CG con pH constante MC (Pasos 4 y 7 y 8), y una simulación MD de carga estática. Al final de este ciclo, se obtienen mAbs mejorados con mayor afinidad de unión.
Los investigadores ampliaron el análisis y probaron las afinidades de unión de estos candidatos con fragmentos de mAbs diseñados por ROSETTA con diferentes variantes de SARS-CoV-2. Los resultados revelaron una afinidad de unión mejorada para los 10 candidatos en comparación con el CR3022 original. Esto indica que todas las moléculas de P01 a P10 pueden inhibir la interacción entre el SARS-CoV-2 y la célula huésped al evitar que RBD esté disponible para unirse a la enzima convertidora de angiotensina 2 (ACE2).
Curiosamente, tanto el CR3022 original como todos los aglutinantes diseñados por ROSETTA mostraron una mayor afinidad de RBD por la variante Omicron del SARS-CoV-2, lo que sugiere que CR3022 y sus mAbs derivados pueden neutralizar la variante Omicron.
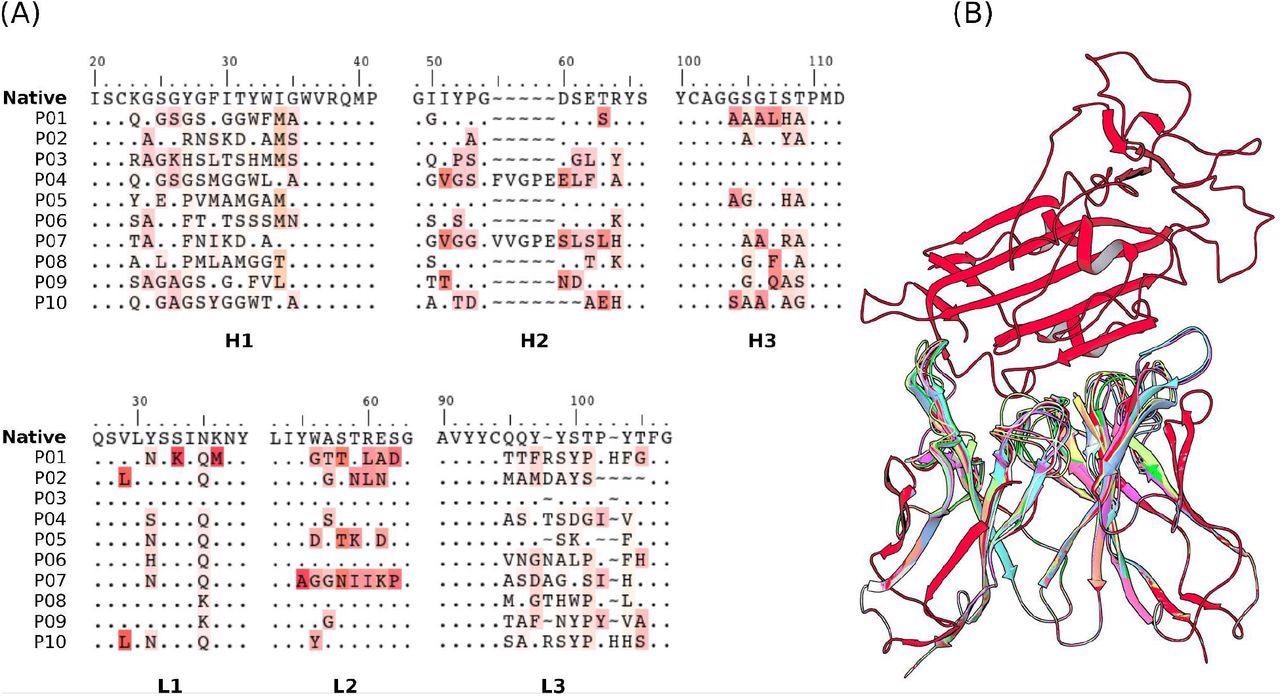
Secuencias de CDR (A) y estructuras (B) de 10 mAbs identificadas para evaluaciones utilizando los métodos US/SIRAH y FORTE. Los puntos representan identidades. Los caracteres restantes en (A) se colorearon de acuerdo con la similitud con sus contrapartes en la secuencia de referencia CR3022 original. En (B), RBD (arriba) se tiñe de rojo y cada anticuerpo candidato (abajo) tiene un color diferente.
Los investigadores evaluaron además la contribución de un aminoácido específico a la unión de RBD a los dos principales aglutinantes, P01 y P06. Esto se logró mediante el uso de escaneo isotópico de alanina (TAS), en el que un aminoácido del candidato potencial se reemplazó por alanina y luego se repitió la simulación compleja para este nuevo aglutinante potencial.
Los resultados de este experimento mostraron que los aminoácidos ubicados en la interfaz Ag-Ab y en lo profundo de la estructura de la proteína son esenciales para el proceso de complejación. Esto se debe a la naturaleza de largo alcance de las interacciones electrostáticas y el acoplamiento electrostático entre conjuntos titulados, que se describen como «epítopos electrostáticos».
Los investigadores también señalan que la carga neta total de mAbs puede afectar la afinidad de unión. Con este fin, encontraron una clara tendencia lineal de los mAbs con menor carga a mostrar una mayor afinidad de unión por RBD. La asociación de los antígenos del SARS-CoV-2 con los mAbs estudiados se derivó de la fuerza culómbica, que también se observó en estudios anteriores.
Conclusiones
En general, el enfoque multiescala utilizado en el estudio actual es una herramienta rápida, robusta y confiable para diseñar mejores ligandos moleculares para identificar el mejor candidato mAb para las variantes del SARS-CoV-2, incluida la variante Omicron. esto es multibanda en silico Por lo tanto, el enfoque es una herramienta razonable y realista para el diagnóstico, tratamiento y prevención del SARS-CoV-2.
*Nota IMPORTANTE
bioRxiv Publica informes científicos preliminares que no han sido revisados por pares y, por lo tanto, no deben considerarse concluyentes, orientar la práctica clínica o el comportamiento relacionado con la salud ni tratarse como información establecida.

«Solucionador de problemas. Gurú de los zombis. Entusiasta de Internet. Defensor de los viajes sin disculpas. Organizador. Lector. Aficionado al alcohol».