Las mitocondrias, los orgánulos productores de energía en las células humanas, alguna vez fueron organismos de vida libre que encontraron su camino hacia las primeras células eucariotas hace más de mil millones de años. Desde entonces, se han integrado a la perfección con sus anfitriones en un ejemplo clásico de evolución simbiótica, y ahora dependen de muchas proteínas producidas en el núcleo de la célula anfitriona para funcionar correctamente.
Las proteínas ubicadas en la membrana externa de las mitocondrias son especialmente importantes; Permiten que las mitocondrias se comuniquen con el resto de la célula, desempeñan un papel en las funciones inmunitarias y en un tipo de muerte celular programada llamada apoptosis. A lo largo de la evolución, las células han desarrollado un mecanismo específico mediante el cual estas proteínas, que se forman en el citoplasma de la célula, pueden insertarse en la membrana mitocondrial. Pero cuál era este mecanismo y en qué están involucrados los jugadores celulares, ha sido durante mucho tiempo un misterio.
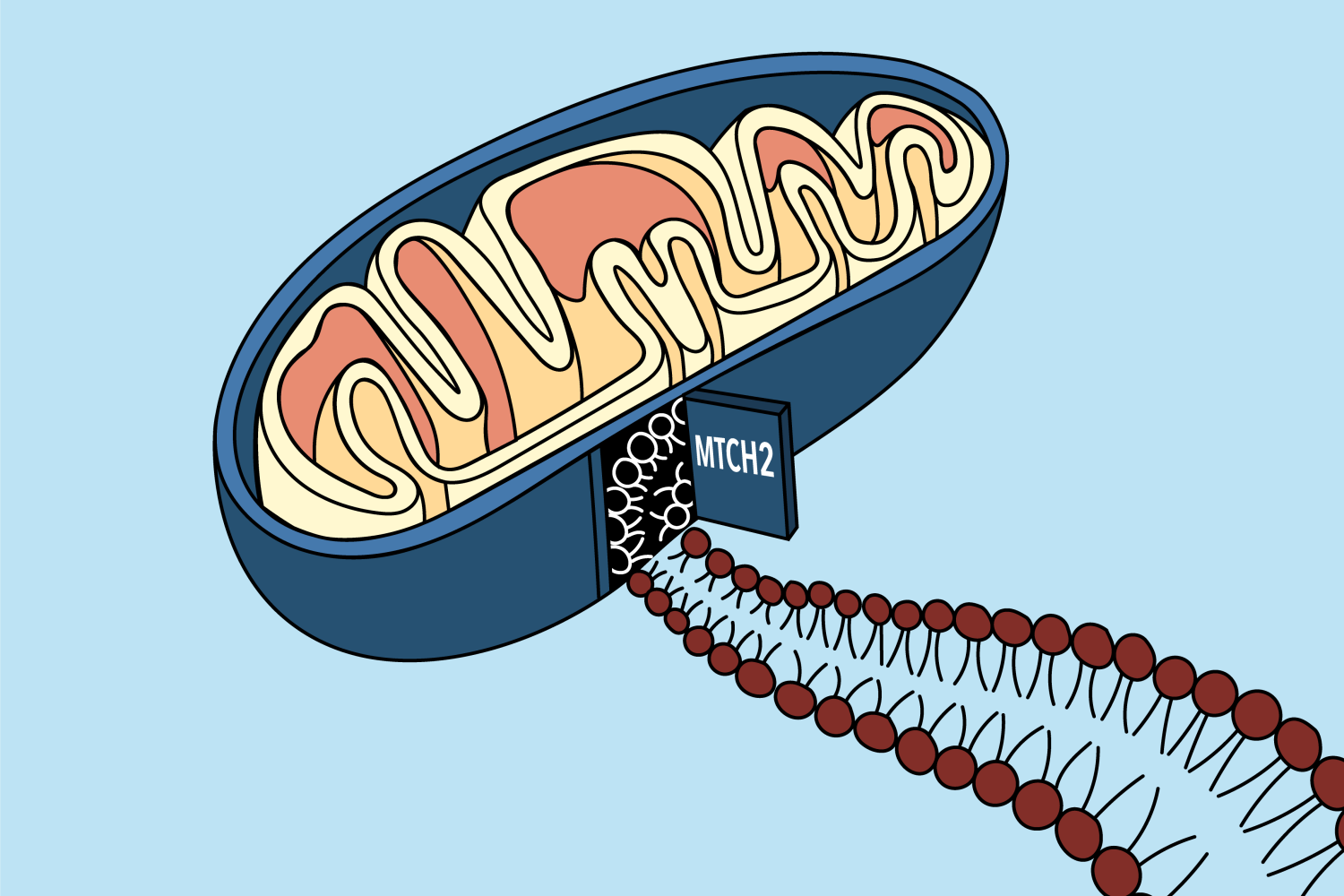
Un nuevo artículo de los laboratorios del profesor Jonathan Wiseman y la profesora de Caltech Rebecca Voorhees ofrece una solución a este rompecabezas. El trabajo fue publicado en la revista el 21 de octubre. Cienciasrevela que una proteína llamada homólogo 2 del transportador mitocondrial, o MTCH2 para abreviar, que se ha relacionado con muchos procesos celulares e incluso enfermedades como el cáncer y el Alzheimer, es responsable de actuar como una ‘puerta’ para que una variedad de proteínas lleguen al membrana mitocondrial.
Weisman, quien también es miembro del Instituto Whitehead de Investigación Biomédica e investigador del Instituto Médico Howard Hughes. «Ha sido un poco misterioso por qué esta proteína única afecta tantos procesos diferentes. Este estudio proporciona una base molecular para comprender por qué MTCH2 está involucrado en la biosíntesis de lípidos, la enfermedad de Alzheimer y la fisión y fusión mitocondrial: porque fue responsable de introducir todos estos diferentes tipos de proteínas en la membrana».
«La colaboración entre nuestros laboratorios fue esencial para comprender la bioquímica de esta interacción y condujo a una nueva comprensión realmente emocionante de una pregunta fundamental en biología celular», dice Voorhees.
Buscando una puerta
Para descubrir cómo se insertan las proteínas desde el citoplasma, específicamente una clase llamada proteínas fijadoras de la cola, en las membranas externas de las mitocondrias, Weismann Lab postdoctorado y primer autor del estudio Alina Guna, junto con el estudiante graduado de Voorhees Lab Taylor Stevens y Alison Inglis decidió, quien es un postdoctorado, utilizó una técnica llamada método de interferómetro CRISPR (o CRISPRi), que fue iniciado por Weissman y sus colaboradores.
“La pantalla CRISPR nos permite eliminar sistemáticamente cada gen y luego mirar y ver qué pasó. [to one specific tail-anchored protein]»Encontramos un gen, MTCH2, cuando nos deshicimos de él hubo una gran caída en la cantidad de proteína que llegaba a la membrana mitocondrial. Así que pensamos, tal vez esa sea la puerta de entrada», dice Guna.
Para confirmar que MTCH2 servía como entrada a la membrana mitocondrial, los investigadores realizaron experimentos adicionales para observar qué sucedía cuando MTCH2 no estaba presente en la célula. Descubrieron que MTCH2 era necesario y suficiente para permitir que las proteínas transmembrana ancladas en la cola se movieran desde el citoplasma a la membrana mitocondrial.
La capacidad de MTCH2 para transportar proteínas desde el citoplasma a la membrana mitocondrial probablemente se deba a su forma especializada. Los investigadores corrieron la secuencia de la proteína a través de Alpha Fold, un sistema de inteligencia artificial que predice la estructura de la proteína a través de secuencias de aminoácidos, lo que reveló que es una proteína hidrofóbica, ideal para insertarse en la membrana lipídica, pero con un surco hidrofílico en otra parte. Las proteínas pueden entrar.
«Es básicamente como un embudo», dice Guna. «Las proteínas provienen del citosol, se deslizan en ese surco hidrofílico y luego viajan desde la proteína hasta la membrana».
Para confirmar que este surco es importante en la función de las proteínas, Guna y sus colegas diseñaron otro experimento. «Queríamos manipular la estructura para ver si podíamos cambiar su comportamiento, y pudimos hacerlo», dice Guna. «Entramos e hicimos una mutación puntual única, y esa mutación puntual fue suficiente para cambiar la forma en que se comporta la proteína y cómo interactúa con los sustratos. Luego continuamos y encontramos las mutaciones que la hacían menos activa y las mutaciones que la hacían es muy activo».
El nuevo estudio tiene aplicaciones más allá de responder una pregunta fundamental para la investigación mitocondrial. «Hay muchas cosas que surgieron de esto», dice Guna.
Por un lado, MTCH2 introduce proteínas esenciales para un tipo de muerte celular programada llamada apoptosis, que los investigadores pueden aprovechar para tratamientos contra el cáncer. «Podemos hacer que las células de leucemia sean más sensibles al tratamiento del cáncer dándoles una mutación que altere la actividad de MTCH2», dice Juna. «La mutación hace que MTCH2 actúe de manera más ‘codiciosa’ y obtenga más cosas en la membrana, algunas de esas cosas con inserciones que son como factores proapoptóticos, por lo que es más probable que esas células mueran, lo cual es excelente en el contexto del tratamiento del cáncer. .»
El trabajo también plantea preguntas sobre cómo MTCH2 ha evolucionado su funcionalidad a lo largo del tiempo. MTCH2 evolucionó a partir de una familia de proteínas llamadas transportadores de solutos, que transportan una variedad de sustancias a través de las membranas celulares. «Estamos realmente interesados en esta cuestión de la evolución, ¿cómo se desarrolla una nueva función a partir de la antigua clase de proteínas ubicuas?» Wiseman dice.
Y los investigadores todavía tienen mucho que aprender sobre cómo las mitocondrias interactúan con el resto de la célula, incluida la forma en que reaccionan al estrés y los cambios dentro de la célula, y cómo las proteínas encuentran su camino hacia las mitocondrias en primer lugar. «Creo que [this paper] Es solo un primer paso «, dice Wiseman. «Esto solo se aplica a una clase de proteínas transmembrana, y no le dice todos los pasos que tienen lugar después de que las proteínas se producen en el citoplasma. Por ejemplo, ¿cómo se transportan a la mitocondria? Así que estén atentos, creo que aprenderemos que ahora tenemos un sistema muy bueno para desbloquear esta parte fundamental de la biología celular».

«Solucionador de problemas. Gurú de los zombis. Entusiasta de Internet. Defensor de los viajes sin disculpas. Organizador. Lector. Aficionado al alcohol».