En un estudio realizado en la Universidad Internacional de Florida, EE. UU., los científicos investigaron el efecto de las mutaciones del dominio de unión al receptor de punta (RBD) de la variante omicron del coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) en su interacción con el convertidor de angiotensina humano. enzima 2 (ACE2).
Los resultados revelan que los cambios estructurales inducidos por la mutación en el omicron RBD conducen a una unión de ACE2 más eficiente. El estudio ya está disponible en bioRxiv* Servidor de preimpresión.
estancia: La importancia de las mutaciones RBD en omicron SARS-CoV-2: desde la apertura de picos hasta el escape de anticuerpos y la unión celular.. Haber de imagen: Ajuste Ztudio/Shutterstock
antecedentes
Poco después de su aparición en Sudáfrica en noviembre de 2021, la variante omicron del SARS-CoV-2 provocó un rápido aumento de los casos de la nueva enfermedad por coronavirus 2019 (COVID-19) en todo el mundo. En comparación con las variantes circuladas anteriormente, la proteína de espinocitosis de la variante omicron contiene más de 30 mutaciones, incluidas 15 específicamente en la mutación RBD. Esto hace que la variante sea más transmisible y resistente a los anticuerpos que las variantes que circulaban anteriormente, incluida la delta.
Actualmente, se han detectado casos de infección por omicron en más de 90 países de todo el mundo. En los EE. UU., la variante omicron reemplazó a delta como variante dominante dentro de las tres semanas posteriores a su descubrimiento. Para comprender el efecto de la variante omicron en la epidemiología de la variante delta, es necesario investigar cómo las mutaciones de la espiga omicron afectan su transmisibilidad y capacidad de escape inmunitario. En este contexto, los estudios han demostrado que la inmunidad inducida por la infección por omicron es suficiente para neutralizar la infección delta.
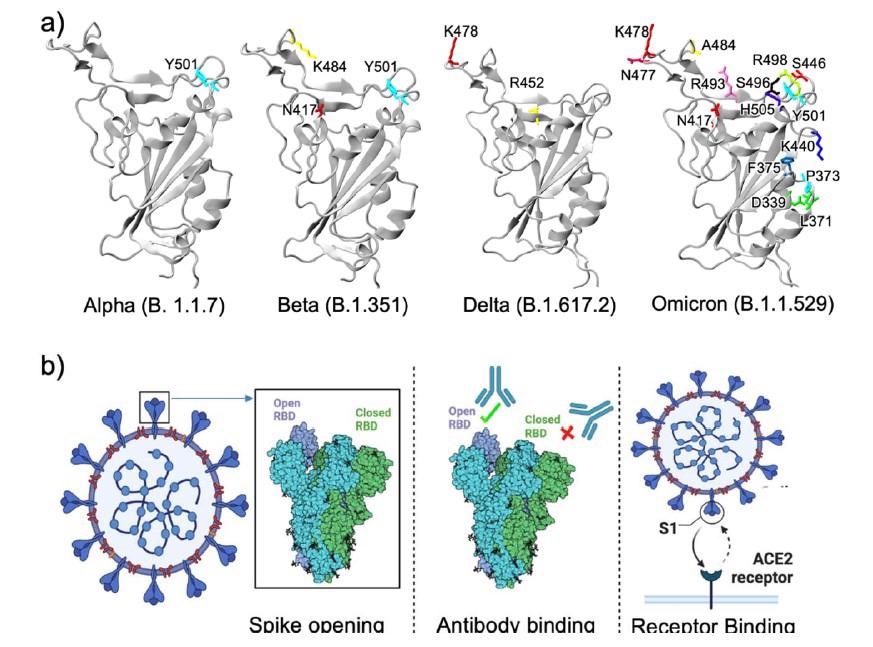
Estructuras RBD de diferentes variantes. Mientras que las variantes Alfa, Beta y Delta tienen menos de tres mutaciones RBD, Omicron tiene una cantidad de mutaciones notablemente alta. b) Tres formas diferentes en las que las mutaciones RBD pueden contribuir a la alta transmisibilidad de una variante (establecido con BioRender.com).
En el estudio actual, los científicos realizaron análisis computacionales para investigar el efecto de las mutaciones de omicron RBD en la unión de ACE2 y las capacidades de escape de anticuerpos.
Los científicos realizaron simulaciones de dinámica molecular de alto RBD para SARS-CoV-2 de tipo salvaje, variantes delta y omicron.
Efecto de las mutaciones en la apertura de RBD
La interacción entre la punta RBD y ACE2 requiere la apertura de la RBD desde el recortador de puntas cerrado. Los enlaces de hidrógeno entre los dominios que conectan los tres RBD en el interruptor de forma cerrada son necesarios para romperse mientras el RBD está abierto.
El análisis realizado en el estudio mostró que la mayoría de los enlaces de hidrógeno de tipo salvaje están en la variante omicron. Sin embargo, se perdió un enlace de hidrógeno inicial (Y505 (A) -F374 (B)) en el omicrón debido a la mutación Y505H. Además, se perdió un ligero enlace de hidrógeno con múltiples residuos debido a una mutación polar en el hidrofóbico S371L. La formación de nuevos enlaces de hidrógeno compensó la abolición del enlace de hidrógeno de tipo salvaje en el omicron. Estas nuevas interacciones facilitaron la apertura del omicron RBD desde la herramienta de corte adjunta.
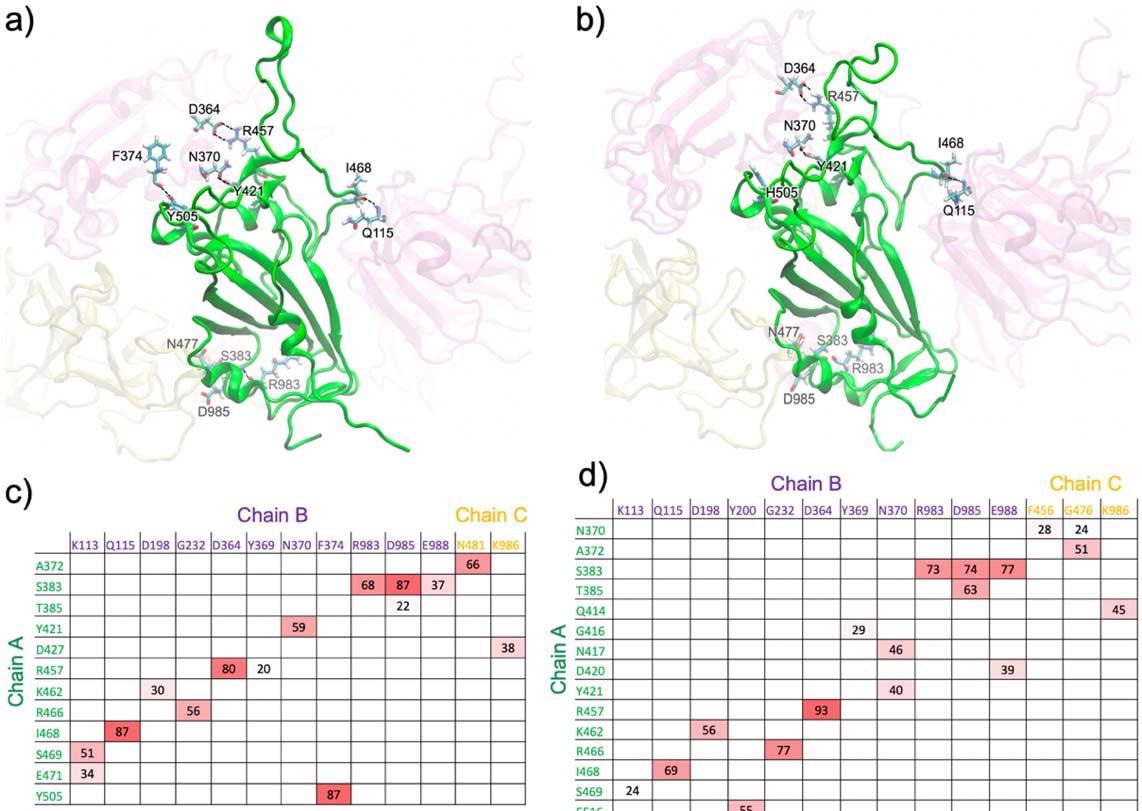
Se formaron enlaces de hidrógeno principales entre el RBD de la cadena A (verde) y los dominios circundantes en la podadora de puntas cerradas para a) WT yb) Omicron. Las interacciones adicionales se muestran en la Figura S1 (desde diferentes puntos de vista). Pares de enlace de hidrógeno y relación de ocupación para c) WT y d) Omicron, con una escala de color de rojo (máximo) a blanco (mínimo).
Efecto de las mutaciones en la estructura de RBD y la unión de anticuerpos
El análisis estructural realizado en el estudio reveló un cambio significativo en la estructura del omicron RBD en comparación con el RBD de tipo salvaje. El cambio estructural primario se observa en la forma que contiene mutaciones polares a hidrofóbicas de S371L, S373P y S375F. Estas mutaciones separaron significativamente los restantes 371 y 375 de la figura, que son sitios de unión de anticuerpos fuertes. Esta segregación de los sitios de unión del anticuerpo puede reducir la eficacia de la unión del anticuerpo, lo que a su vez puede facilitar que la variante omicron escape de la neutralización mediada por anticuerpos. Un análisis adicional reveló que casi todos los mutantes RBD de omicron están ubicados en epítopos importantes, lo que justifica la alta capacidad de escape inmunitario de omicron.
El estudio identificó tres epítopos en el omicron RBD donde las mutaciones causaron una inducción significativa de antígenos en comparación con los epítopos de tipo salvaje. Los cambios antigénicos inducidos por la mutación observados en el omicron RBD podrían reducir significativamente la sensibilidad de los anticuerpos de tipo salvaje a estos epítopos. Sin embargo, estos epítopos pueden inducir una respuesta inmunitaria más robusta debido al aumento del antígeno.
Efecto de las mutaciones en la unión de ACE2 ارتباط
El motivo de unión al receptor (RBM) del omicron contiene 10 mutaciones. Para investigar el efecto de estas mutaciones en la interacción omicron RBD-ACE2, en el estudio se realizaron simulaciones de dinámica molecular del complejo RBD-ACE2.
Los resultados revelaron que el enlace de hidrógeno entre proteínas en el omicrón es mucho mayor que en el delta, lo que indica una interacción más fuerte entre el omicrón RBD-ACE2. Se han identificado cuatro pares de enlaces de hidrógeno con más del 70% de ocupación en el complejo omicron RBD-ACE2. Por el contrario, solo se ha identificado un par de enlaces de hidrógeno delta. Estos resultados indican que las interacciones interfaciales en el omicrón son mucho más fuertes que las del delta.
En comparación con el virus de tipo salvaje, la variante omicron mostró enlaces de hidrógeno únicos adicionales en la interfaz RBD-ACE2. Por el contrario, no se observó ningún enlace de hidrógeno adicional en la variante delta. En general, estos resultados indican una interacción omicron RBD-ACE2 más eficiente y estable debido al aumento de las interacciones interfaciales.
Estudia la importancia
Los resultados del estudio revelaron que omicron RBD tiene una mayor afinidad de unión por ACE2 que delta RBD. Además, las mutaciones en los epítopos omicron de RBD clave pueden reducir la sensibilidad a la unión de anticuerpos, lo que a su vez puede aumentar la aptitud inmunitaria de la variante.
*Nota IMPORTANTE
bioRxiv Publica informes científicos preliminares que no han sido revisados por pares y, por lo tanto, no deben considerarse concluyentes, orientar la práctica clínica o el comportamiento relacionado con la salud ni tratarse como información establecida.

«Solucionador de problemas. Gurú de los zombis. Entusiasta de Internet. Defensor de los viajes sin disculpas. Organizador. Lector. Aficionado al alcohol».