Un ejemplo de una micrografía con una distribución irregular de nieve donde las partículas son eliminadas por el recogedor automático. crédito: fuente de luz de diamante
La tecnología Cryo-EM requiere que las muestras de proteínas se congelen antes de obtener imágenes con microscopía electrónica. Esta técnica revolucionaria y su aplicación en biología estructural fue el foco del Premio Nobel de Química en 2017 y contribuyó a una ola de nueva información estructural para proteínas que era difícil o imposible de preparar para la cristalografía de rayos X. Dado que la crio-EM se está volviendo cada vez más popular, han surgido nuevos métodos y herramientas para mejorar la técnica y hacerla más eficiente. Ahora, muchas personas están trabajando en la forma en que se preparan las muestras para que sea fácil obtener información estructural de alta resolución de cada experimento. Una vez que se preparan las muestras, se han desarrollado una serie de herramientas automatizadas para seleccionar partículas congeladas para su procesamiento. Fue durante la investigación de estas herramientas que Ph.D. Con la ayuda de Yuri Chaban y Donovan Webb, el estudiante Mateusz Olek y su supervisor Bijon Zhang descubren un problema inusual. Sus hallazgos fueron publicados en la revista estructura.
Puntos ciegos de la automatización
Los recolectores de partículas automatizados están diseñados para analizar una imagen y seleccionar automáticamente las mejores partículas para elegir para los experimentos. Mientras estudiaba el rendimiento de estas herramientas, el equipo notó partes de la imagen sin selecciones. Estos vacíos no se explicaban fácilmente, especialmente cuando el equipo examinó las imágenes a simple vista y vio claramente que las partículas estaban presentes. Por alguna razón, los recolectores automáticos de partículas estaban ciegos a ciertas áreas de la imagen. Este problema podría tener repercusiones para los experimentos crio-EM. Si los programas de automatización dejan partículas viables, es posible que los científicos no puedan recopilar todos los datos que necesitan para realizar un experimento.
El equipo pronto notó que el fondo de las fotos no era consistente. Algunas partes eran más oscuras, otras más claras. Esto podría explicar algunas fallas en los programas de automatización que se basan en medir la variación de la molécula de proteína en el contexto. Para hacer el enfriamiento EM, las moléculas de proteína se suspenden en una fina capa de hielo, por lo que el equipo concluyó que los contrastes en el fondo de la imagen están relacionados con diferentes espesores de hielo. Esto planteó varios problemas para los investigadores que utilizan el dispositivo cryo-EM. Primero, una solución obvia es intentar que la película de hielo sea más uniforme. Desafortunadamente, aunque se están haciendo grandes esfuerzos para mejorar la preparación de muestras criogénicas de EM, todavía es muy difícil crear una película uniforme de hielo. A menudo se puede ver un gradiente de espesor de hielo en una muestra crio-EM.
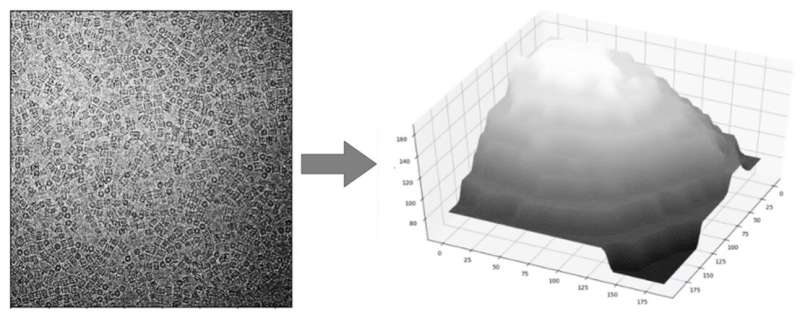
La distribución del espesor del hielo se estima por micrografía. crédito: fuente de luz de diamante
empezar desde cero
Matthews y el equipo comenzaron desde cero para desarrollar una nueva forma de combatir el problema del hielo. Comenzaron por dividir las diferentes imágenes y analizar el fondo. Esto permitió que su recolector identificara las partículas independientemente del fondo proveniente del hielo. Esta innovación significó que en un experimento dado, los investigadores ahora podían recopilar de manera confiable más información estructural mediante el análisis de más moléculas de proteína. Sin embargo, este no fue el final del camino. Si bien recolectar más partículas es de gran valor para los investigadores que utilizan crio-EM, la cantidad de hielo afecta la calidad de las partículas y, por lo tanto, la calidad de los mapas crio-EM que se pueden reconstruir. Matthews y el equipo de investigación sabían que podían hacer avanzar el software al proporcionar a los investigadores información inmediata sobre la calidad de las moléculas de proteína fotografiadas.

La distribución del espesor del hielo se estima por micrografía. crédito: fuente de luz de diamante
En su última publicación, el equipo de investigación destaca dos problemas principales que pueden surgir cuando el hielo no tiene el grosor óptimo. En primer lugar, el hielo muy espeso provoca más ruido de fondo en la imagen. Esto dificulta la obtención de datos de alta resolución de una molécula de proteína. Por el contrario, si la película de hielo es demasiado delgada, es posible que no soporte adecuadamente las proteínas. Este problema depende en gran medida de las proteínas específicas que el investigador está analizando. Por ejemplo, algunas proteínas son pequeñas y están fuertemente unidas en una configuración globular. Estas proteínas se pueden sostener en capas de hielo relativamente delgadas. Sin embargo, muchas proteínas son grandes y tienen ramificaciones largas y prominentes que pueden caer fuera de la capa de hielo si es demasiado delgada. Esto significa que el hielo delgado dificulta la visualización de este tipo de proteínas, incluso si el ruido de fondo es muy bajo. El grosor óptimo del glaseado es algo que minimiza el fondo pero que es lo suficientemente grueso como para soportar completamente la proteína. El espesor óptimo del hielo a menudo depende de la naturaleza proteína En estudio y cambiará dependiendo de la experiencia.

Comparación de micrografías antes y después de la ecualización de contraste. crédito: fuente de luz de diamante
Su nueva herramienta de software, IceBreaker, puede automatizar completamente la selección de partículas. Sin embargo, el equipo eligió un enfoque que brinda más flexibilidad a los investigadores que lo utilizan. En lugar de tomar decisiones, el software comenta cada parte, lo que le da al investigador una indicación de calidad. Esto les permite orientar sus experiencias precisamente de la manera que necesitan para lograr los mejores resultados. A veces, son suficientes menos partículas de alta calidad y, a veces, se necesitan más partículas de baja calidad del hielo grueso para mostrar tendencias moleculares únicas que no son compatibles con el hielo delgado. Con el nuevo software IceBreaker, los investigadores tienen el control total de los datos que recopilan. IcreBreaker ahora se está implementando como parte de la canalización de recopilación de datos de Diamond. Centro de Imágenes Bioelectrónicas (eBIC) Está disponible de forma gratuita en GitHub.
Mateusz Olek et al., IceBreaker: un programa para crio-EM de una sola partícula de alta resolución con hielo irregular, estructura (2022). DOI: 10.1016 / j.str.2022.01.005
Introducción de
fuente de luz de diamante
La frase: Solving the Ice Problem in Cryoelectron Microscopy (14 de febrero de 2022) Recuperado el 14 de febrero de 2022 de https://phys.org/news/2022-02-ice-problem-cryo-electron-microscopy.html
Este documento está sujeto a derechos de autor. Sin perjuicio de cualquier trato justo con fines de estudio o investigación privados, ninguna parte puede reproducirse sin permiso por escrito. El contenido se proporciona únicamente con fines informativos.

«Solucionador de problemas. Gurú de los zombis. Entusiasta de Internet. Defensor de los viajes sin disculpas. Organizador. Lector. Aficionado al alcohol».

